ProteoGenix a développé la lignée XtenCHOTM, le système d’expression le plus productif du marché pour la production transitoire d’anticorps monoclonaux, qui surpasse même les performances des cellules ExpiCHO. Basée sur des années de recherche, notre lignée propriétaire XtenCHOTM vous donne accès à des rendements de production d’anticorps recombinants de plus de 1 g/L à des prix imbattables.
Pourquoi choisir ProteoGenix pour la production de vos anticorps monoclonaux ?

XtenCHOTM > ExpiCHO
Notre système d’expression propriétaire surpasse même les rendements des cellules ExpiCHO.

Des prix imbattables
1 mg d’anticorps purifiés* pour seulement 730 € grâce aux performances exceptionnelles des cellules XtenCHOTM

Quantité garantie
Nous vous garantissons la livraison de la quantité commandée ou prix indiqué dans le devis.

Un grand choix de systèmes d’expression
Produisez vos anticorps dans des systèmes d’expression HEK ou CHO.

Experts en ingénierie d’anticorps
Humanisation, maturation d’affinité, développement d’anticorps bispécifiques…Générez les variants d’anticorps qui feront la réussite de votre projet.

Des délais courts
De la séquence de votre gène à votre anticorps en seulement 3 à 4 semaines.
Contenu de notre service de
production d’anticorps recombinants
| Étape | Contenu | Délai | Livrables |
|---|---|---|---|
| Séquençage de l’anticorps monoclonal |
|
2 à 3 semaines pour les régions variables et les séquences leader 3 à 4 semaines pour l’anticorps complet |
|
| Synthèse et clonage des gènes |
|
2 à 3 semaines |
|
| Production d’anticorps monoclonal + purification |
|
À partir de 3 à 4 semaines |
|
Options disponibles (liste non exhaustive) :
|
|||
XtenCHOTM: l’étalon or des systèmes d’expression pour la production d’anticorps monoclonaux
ProteoGenix offre un système d’expression transitoire à haute performance exclusif avec des rendements en anticorps monoclonaux supérieurs à 1 g/L. Grâce à notre protocole de transfection maison Xten et à notre lignée cellulaire propriétaire XtenCHOTM , notre système d’expression en cellules de mammifère surpasse même les performances du système ExpiCHO, la lignée d’expression transitoire la plus productive du marché.
Notre système d’expression Xten est notre solution pour tous vos problèmes de production d’anticorps recombinants. Cerise sur le gâteau, il permet une réduction considérable des coûts de production.
Voici quelques exemples des résultats incroyables que nous avons obtenus pour l’expression transitoire du pembrolizumab et d’une IgG humaine.
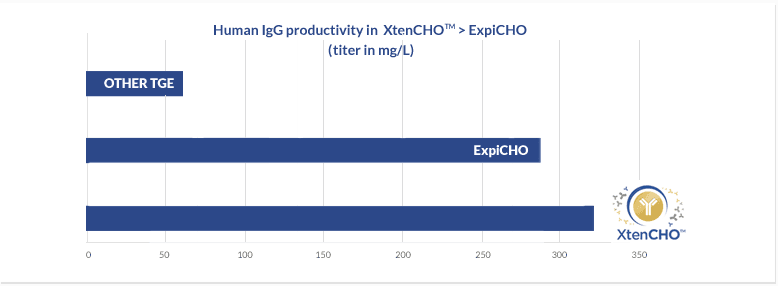
Comparaison des rendements de l’expression d’une IgG humaine dans trois systèmes d’expression différents,
dont XtenCHOTM avec le protocole de transfection Xten.
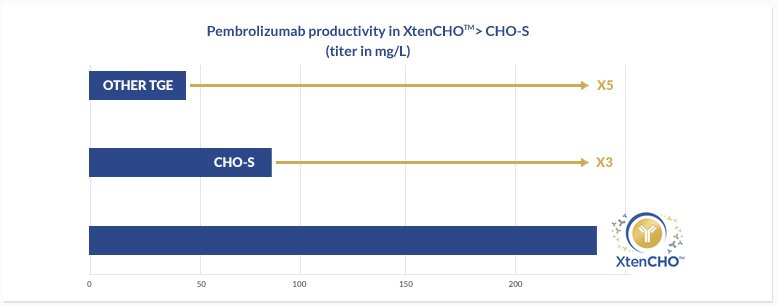
Comparaison des rendements de l’expression du pembrolizumab dans trois systèmes d’expression différents,
dont XtenCHOTM avec le protocole de transfection Xten.
Étude de cas : Production d’anticorps recombinant pembrolizumab
OBJECTIF DE L’ÉTUDE
Produire le pembrolizumab, un anticorps thérapeutique recombinant, dans notre système d’expression propriétaire Xten.
GÈNES ET VECTEURS D’EXPRESSION
Les gènes codant pour la chaîne lourde (HC) et la chaîne légère (LC) du pembrolizumab ont été chimiquement synthétisés et optimisés pour l’expression en cellules CHO. Les gènes ont été clonés dans le vecteur d’expression en cellules de mammifère propriétaire pTXs1 de ProteoGenix. La carte du vecteur se trouve dans le rapport PDF.
TESTS DE PRODUCTION ET DE PURIFICATION DE L’ANTICORPS MONOCLONAL À PETITE ÉCHELLE
Après la réalisation d’une préparation exempte d’endotoxines de l’ADN des constructions d’expression dans pTXs1, les constructions ont été transfectées transitoirement dans des cellules XtenCHO propriétaires selon le protocole de transfection propriétaire XtenTM . Après le recueil du milieu de culture, le rendement de la production de l’anticorps a été déterminé par analyse sur un système Octet Red. L’anticorps recombinant a ensuite été purifié par affinité vis-à-vis de la protéine G.
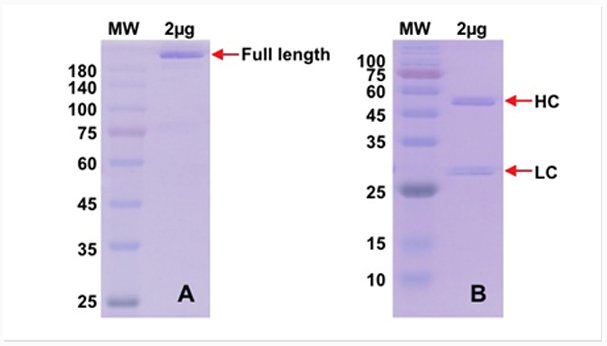
Contrôle de la qualité du pembrolizumab purifié. Coloration au bleu de Coomassie.
A. SDS-PAGE en condition non réductrice. B. SDS-PAGE en condition réductrice.
RÉSULTATS DE L’EXPRESSION DE L’ANTICORPS PEMBROLIZUMAB
| Anticorps | Rendement | Pureté |
|---|---|---|
| Pembrolizumab | 235 mg/L | >95% |
Quels sont les bénéfices de
la production d’anticorps monoclonaux ?
La production d’anticorps monoclonaux par la technologie de l’expression recombinante a été une avancée majeure dans le domaine du développement d’anticorps thérapeutiques de par les avantages de cette technologie par rapport à la méthode « traditionnelle » de production d’anticorps à partir d’hybridomes.
Reproductibilité, contrôle et sécurité
La production d’anticorps monoclonaux destinés à des applications thérapeutiques requiert un haut niveau de contrôle et de reproductibilité. Comme des paramètres cruciaux, tels que la séquence d’ADN et la séquence protéique, sont chimiquement définis, la production d’anticorps recombinants permet de créer un procédé standardisé pour la production d’anticorps monoclonaux, avec de très faibles variations d’un lot à l’autre. Étant donné que la production d’anticorps recombinant commence avec une séquence d’ADN connue, les mutations ou les dérives de lignée cellulaire qui peuvent se produire dans les lignées d’hybridome sont également évitées.
Grande pureté
La production d’anticorps recombinants conduit à un haut degré de pureté grâce à l’absence de contaminants sériques.
Ingénierie et reformatage
La production d’anticorps monoclonaux recombinants permet d’accéder au contrôle de la structure de l’anticorps au niveau génétique. Cela est particulièrement important s’agissant du développement d’anticorps thérapeutiques, car cela permet de moduler les propriétés pharmacologiques moduler les propriétés pharmacologiques d’un anticorps.
La possibilité de modifier le gène à exprimer dans un système d’expression sélectionné donne également accès à des possibilités infinies de solutions en matière de :
- reformatage : commutation d’espèce, d’isotype ou de sous-classe,
- ingénierie d’anticorps : humanisation d’anticorps monoclonaux, maturation d’affinité, anticorps bispécifiques, conjugués anticorps-médicament (ADC), fragments d’anticorps (Fab, Fab2, scFv).
Pas d’utilisation d’animaux
De nos jours, une attention grandissante est apportée aux questions éthiques et au bien-être des animaux. Grâce à la technologie de l’expression recombinante, le processus de production d’anticorps peut entièrement s’opérer sans aucune utilisation d’animaux.
Expression transitoire ou stable ? Quel service de production
d’anticorps monoclonaux devriez-vous choisir ?
Choisir la solution la plus appropriée pour la production de votre anticorps monoclonal peut avoir un impact majeur sur divers aspects de votre projet tels que sa durée. La courte section suivante est destinée à vous aider à faire votre choix entre expression transitoire et expression stable.
Le principal avantage de la production d’anticorps monoclonaux est que cette méthode permet la production rapide d’une quantité relativement importante d’anticorps. Cependant, dans une transfection transitoire, le gène transfecté ne s’intègre pas dans le génome de la cellule hôte et peut être perdu par la cellule au bout de quelques jours. Cette solution convient donc surtout pour les applications à court terme telles que la production d’une protéine à petite échelle.
La génération de lignées cellulaires stables implique l’intégration d’un gène synthétique dans le génome de la cellule hôte du système d’expression. Comme ce processus de développement peut être long et compliqué (plus de trois mois), les lignées cellulaires stables sont surtout choisies pour les applications à long terme telles que la production d’anticorps thérapeutiques. Pour la production à grande échelle, les lignées cellulaires stables permettent d’élaborer un procédé de production standardisé garantissant des rendements élevés et un meilleur contrôle de la qualité.
Si vous souhaitez en savoir davantage, n’hésitez pas à contacter l’un de nos chargés d’affaires qui se fera un plaisir à vous aider à choisir la solution de production d’anticorps la mieux adaptée à votre projet.
*at least 4 antibodies
